با وجود پیشرفت های اخیر در روش ها و مواد جراحی ، تقریباً 25٪ از آسیب های روتاتور کاف بهبود نمی یابند. کلینیک مایو در حال پیگیری رویکرد پزشکی احیا برای بهبود درمان این آسیب های ناتوان کننده است.
دکتر جان می گوید: “ما از 20 سال گذشته از نظر مهندسی مکانیک ، با انواع جدیدی از آنکور، مواد بخیه و روش های جراحی ، راهی طولانی طی کرده ایم. اما اکنون متوجه شده ایم که این مشکل مکانیکی نیست – بلکه از نظر زیست شناختی است.”
بازسازی روتاتور کاف با استفاده از پچ electrospun
مرکز پزشکی احیا مایو در حال توسعه الیاف الکترواسپونی است که با جراحی می توانند باعث بهبودی تاندون شوند. محققان با ایجاد ساختارهای الیافی در آزمایشگاه که از تاندون طبیعی الگو می گیرد ، از مدل های حیوانی برای بررسی روش های جاسازی محصولات فاکتور رشد در این تکه ها استفاده می کنند.
دکتر توکیش می گوید: “به دلیل انقلاب ارتوبیولوژیک ، ما در حال درک علوم پایه ای هستیم که دقیقاً نشان دهنده یک تاندون برای بهبود است.” “ما آموخته ایم كه می توانیم مواد كمكی را اضافه كنیم كه محیط بیوشیمیایی لازم را برای احیای مجدد آن تاندون فراهم می كند. قبلاً این داستان علمی تخیلی بود. اما در حال حاضر ، حداقل در آزمایشگاه ، این به وقوع پیوسته است.”
ترویج ترمیم و بازسازی تاندون
الکترواسپینینگ برای ایجاد الیافی استفاده می شود که مانند الیاف تاندون روی سطح نانو اندازه گیری می شوند. الیاف را می توان در جهات مختلف قرار داد.
دکتر توکیش می گوید: “ما می دانیم که توانایی بازسازی بافتها اغلب به جهت فیبرهای آنها بستگی دارد.” “الکترواسپینینگ به ما امکان می دهد موادی را که معمولاً مورد استفاده قرار می گیرند و از نظر زیست شناختی پذیرفته می شوند ، درون یک میدان مغناطیسی قرار دهیم. بسته به قدرت میدان آهنربا و جهت چرخش آن ، می توانیم نانوالیاف را به صورت لایه لایه به موازات یکدیگر یا با هم تلاقی کنیم ، یا واقعاً در آزمایشگاه می توانیم از تعدادی از این زمینه های مختلف مکمل برای ایجاد ساختاری که تاندون بومی را تقلید می کند استفاده کنیم. “
ترکیبات مختلفی از الیاف در مدل های موش صحرایی آزمایش شده است که همراه با دانشگاه ایالتی آریزونا تولید شده اند. قبل از قرار دادن در مدل ها ، تکه های فیبر با محصولات مختلف فاکتور رشد آغشته شده اند.
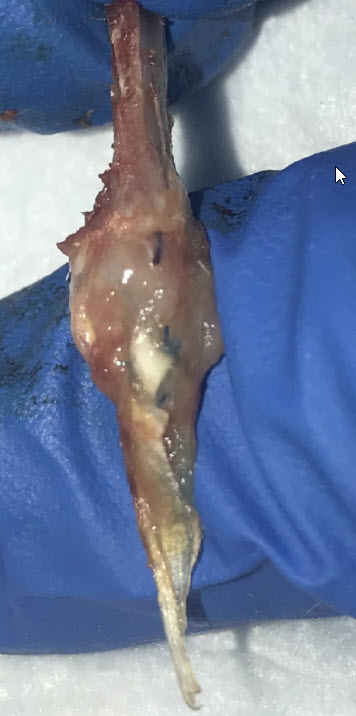
دکتر توکیش می گوید: “آنچه واقعاً هیجان انگیز است این است که ما می توانیم وصله را از قبل در عواملی که مکمل ناحیه تاندون های جداگانه مورد نیاز ما هستند خیس کنیم.” “اگر عضله باشد ، می توانیم عواملی را تقویت کنیم که باعث رشد عضله در آن ناحیه از وصله شود. اگر این لایه غضروف کلسیفیه شده روی استخوان باشد ، می توانیم عواملی را ترغیب کنیم که این نوع بازسازی را در آن قسمت از پچ ترغیب می کند.”
علاوه بر تأمین فاکتورهای رشد لازم ، مواد کمکی به خوبی قادر به تغییر محیط بیوشیمیایی تاندون هستند. دکتر توکیش می گوید: “ما آموخته ایم که این مواد می توانند سلول های سیگنال دارویی بدن خود را برای جذب در ناحیه آسیب دیدگی یا پارگی تحلیل برنده تشویق کرده و محیط لازم را برای بازسازی تاندون فراهم کنند.” “هنگامی که ما در نهایت توانستیم وصله را به بیماران انسانی وارد کنیم ، ممکن است به عنوان داربست عمل کند تا علاوه بر ترمیم بلکه بازسازی را نیز تشویق کند.”
هدف استفاده از این سیستم برای درمان تاندونوپاتی شدید است. دکتر توکیش می گوید: “در بیماران مبتلا به پارگی جبران ناپذیر ، وصله به تنهایی یا همراه با سایر فناوری هایی که در حال حاضر استفاده می کنیم ممکن است به ترکیب تاندون جدید در بدن و بیماران برای بازیابی عملکرد قبلی کمک کند.”
برای بیماران با تاندون هایی که به شدت آسیب دیده و هنوز قابل ترمیم هستند ، سیستم بیولوژیک ممکن است باعث بهبودی و محافظت از ترمیم جراحی شود. “بسیاری از بیماران در جمعیت شناسی جوان – بین 40 تا 60 سال – که دارای تاندونوپاتی هستند که به سختی قابل درمان هستند ، می بینیم. متأسفانه ، آرتروپلاستی معکوس شانه ، که انقلابی در مراقبت از بیماران مسن ایجاد کرده است ، دکتر توکیش می گوید ، گزینه خوبی برای افراد جوان است. “ما هنوز چند روش با آزمایشات انسانی فاصله داریم. اما احساس می کنیم که تقویت ترمیم تاندون از طریق قسمت پزشکی احیا ممکن است کلید گمشده باشد که به ما کمک می کند تا اشکهای روتاتور کاف را بهتر درمان کنیم.”
